采美网 采美网 2022-11-17 11:05:32 1215
‡
人体是由许许多多奇妙的复杂功能构成的,它们让你感到蓬勃的的生命力。我们越了解这些功能,越明白如何保持其平稳运行。
比如说,线粒体、皮肤和衰老,大多数人可能不会把他们联系到一起,但其实线粒体功能、皮肤健康和抗衰老是紧密相连的。
尽管线粒体是我们细胞中一个小小的细胞器,但它的功能异常强大。研究表明,身体中线粒体的健康状况可能决定了你的皮肤是否处于良好状态。
线粒体是什么?
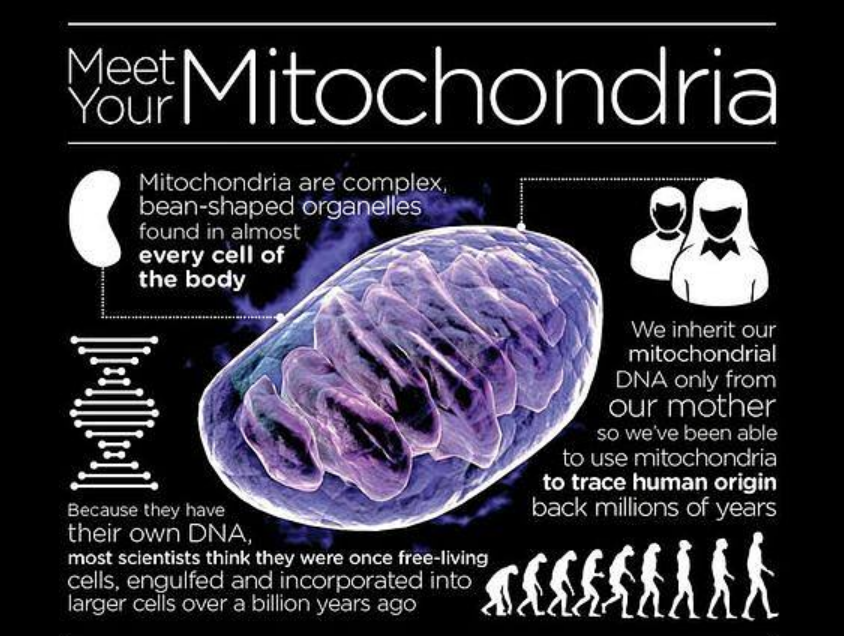
线粒体存在于所有动植物和具有复杂细胞结构的生物的细胞中,一些细胞只包含一个线粒体,而有些细胞(如肌肉细胞)可能包含数千个。
线粒体由外至内可划分为线粒体外膜(OMM)、线粒体膜间隙、线粒体内膜(IMM)和线粒体基质四个功能区。
1、线粒体外膜较光滑,起细胞器界膜的作用。膜上包含酶和线粒体蛋白质,允许小分子通过。
2、线粒体内膜则向内皱褶形成线粒体嵴,增加了可用于化学反应的表面积,容纳蛋白质,是ATP合成的场所。
3、内外膜之间的空间是膜间隙。
4、被线粒体内膜包裹的是线粒体基质。在线粒体基质和内膜中,有数百种酶。这些酶对ATP的生产很重要。线粒体DNA也位于基质中。通常来说,细胞DNA主要存在于细胞核中,但线粒体有自己的DNA,与核DNA一样,线粒体DNA(mtDNA)保存着许多蛋白质和基因的信息,让它能发挥更多重要作用。
‡
线粒体的功能是什么?
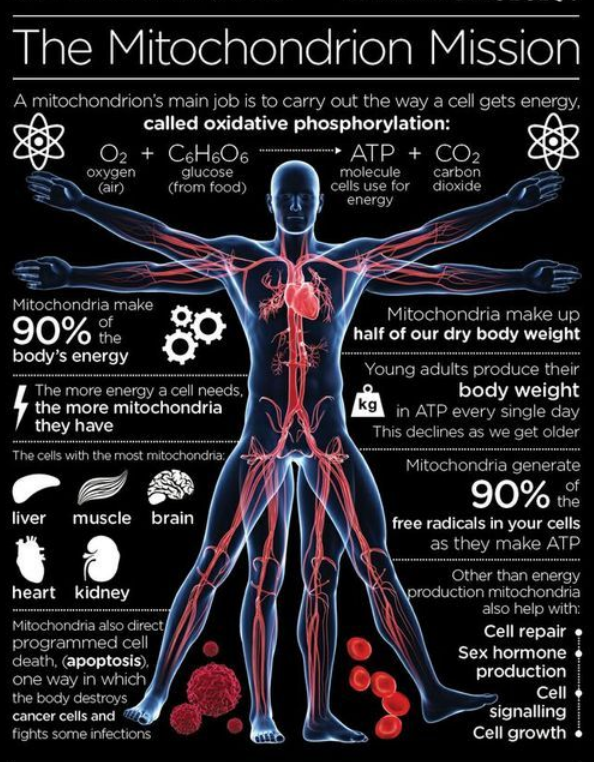
线粒体是细胞的“能量站”,能将我们吃进去的食物中的糖、脂肪或蛋白质分子转化为我们身体可以使用的能量。具体来说,线粒体是“氧化磷酸化”或“细胞呼吸”的场所,在这个过程中,线粒体生产出我们身体中大部分的三磷酸腺苷(ATP)——一种存在于所有生物中的非常复杂的有机化学物质。
随着年龄的增长,线粒体功能可能开始下降。研究表明,线粒体功能障碍与阿尔茨海默病、帕金森病和癌症有关。
线粒体也在细胞死亡或凋亡中发挥作用。
‡
线粒体与皮肤老化的关系
线粒体疾病及功能障碍与衰老有关。
在生产能量时,线粒体中同时也产生了活性氧(ROS)。活性氧是高度带电的粒子,可以破坏DNA、脂肪和蛋白质。
研究表明,“羟基自由基是最具破坏性的活性氧,因为它具有高度活性,对细胞中几乎每种分子类型都会造成氧化损伤,包括脂质、蛋白质和核酸。”
当活性氧产生量较高时,线粒体DNA会受到氧化损伤,突变率会高得多。当线粒体DNA突变增加 时,线粒体的正常功能减少,皮肤老化的迹象,如细纹、皱纹和变色也就可能出现了。
并且,线粒体DNA一旦被活性氧损伤,这些损伤在细胞增殖时也会被复制。随着时间的推移,受损细胞越来越多,老化也就会进一步加速。
另外,有更多的证据证明,线粒体功能障碍和氧化应激导致皮肤光老化。光老化是皮肤的过早老化,是由于反复暴露在紫外线辐射(UV)下导致。
在一项研究中,表皮角质形成细胞或皮肤最外层的细胞对线粒体功能障碍和紫外线辐射更敏感。这项研究表明,两周的阳光照射(尤其是UVA辐射)可导致真皮常见“缺失”增加40%。这种情况可能持续16个月。
而当线粒体功能正常时,以上过程都不容易出现,衰老过程就是正常且缓慢的。
‡
如何保持线粒体健康
改善线粒体的健康可以改善我们器官、皮肤和整个身体的健康,同样也有助于延缓皮肤老化。我们可以做一些事情来保持线粒体的健康。
研究表明,少糖、低碳水的健康饮食可以改善线粒体功能,而摄入大量碳水化合物可能会增加体内自由基和其他毒素的产生。这是因为生酮饮食(摄取高比例脂肪、低比例碳水化合物、蛋白质和其他营养的饮食方式)能促进线粒体的生成并抵消大量氧化应激,从而减少对线粒体的损伤。
定期锻炼和避开环境中的毒素是确保线粒体功能正常的其他方法。例如,在室外涂上防晒霜,尽量缩短暴露在紫外线下的时间,以减小紫外线对线粒体的潜在损害。
另外,也可以通过一些科学技术来对已经受损的线粒体进行修复。
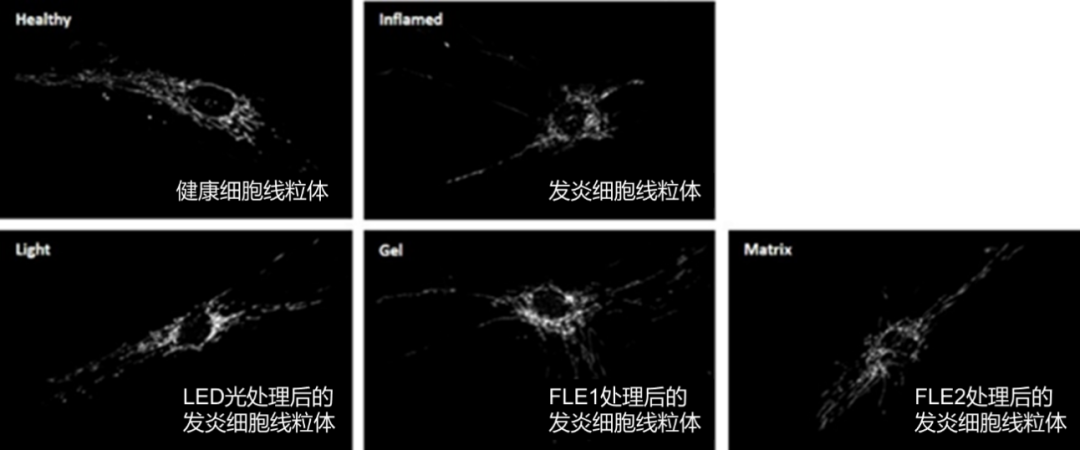
例如,FLE线粒体再生荧光治疗通过斯托克斯位移现象产生覆盖465-750nm的动态超脉冲多波长荧光光谱,靶向作用于受损线粒体,照射5分钟即可使发炎细胞中的受损线粒体数量、结构及功能恢复到正常状态。
‡
总 结
1、线粒体通常被称为细胞的能量工厂,因为它们能够将 食物中的能量转化为我们身体可用的能量。
2、生成ATP以产生能量是线粒体的主要作用,这发生在一个叫做细胞呼吸的过程中。
3、线粒体结构复杂,有两层膜。它们携带着控制数种蛋白质和基因的DNA信息。
4、线粒体功能障碍与阿尔茨海默病、帕金森病和癌症等疾病有关。当线粒体功能不正常时,衰老过程加快。
5、根据研究,线粒体功能障碍可导致光老化,尤其是当皮肤暴露于紫外线辐射时。
6、为了避免线粒体功能障碍,我们需要均衡饮食,使用适当的补剂,以及利用先进科技,以维持皮肤的健康。
参考文献
▼ ▼ ▼
向上滑动阅览
1. Siekevitz, P. (1957). Powerhouse of the cell. Scientific American, 197(1), 131-144. Abstract: https://www.jstor.org/stable/24940890?seq=1#page_scan_tab_contents2. Cooper, T. G., & Beevers, H. (1969). Mitochondria and glyoxysomes from castor bean endosperm Enzyme constituents and catalytic capacity. Journal of Biological Chemistry, 244(13), 3507-3513. Full Text: https://www.ncbi.nlm.nih.gov/books/NBK9896/3. Berg, J. M., Tymoczko, J. L., & Stryer, L. (2002). The respiratory chain consists of four complexes: three proton pumps and a physical link to the citric acid cycle. Biochemistry, 5, 320-323. Full Text: https://www.ncbi.nlm.nih.gov/books/NBK21163/4. Jonckheere, A. I., Smeitink, J. A., & Rodenburg, R. J. (2012). Mitochondrial ATP synthase: architecture, function and pathology. Journal of inherited metabolic disease, 35(2), 211-225. Full Text: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3278611/5. Chan, D. C. (2006). Mitochondria: dynamic organelles in disease, aging, and development. Cell, 125(7), 1241-1252. Full Text: https://www.sciencedirect.com/science/article/pii/S00928674060076896. Weinberg, S. E., & Chandel, N. S. (2015). Targeting mitochondria metabolism for cancer therapy. Nature chemical biology, 11(1), 9. Full Text: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4340667/7. Elmore, S. (2007). Apoptosis: a review of programmed cell death. Toxicologic pathology, 35(4), 495-516. Full Text: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2117903/8. Bratic, A., & Larsson, N. G. (2013). The role of mitochondria in aging. The Journal of clinical investigation, 123(3), 951-957. Full Text: https://www.jci.org/articles/view/641259. Naidoo, K., Hanna, R., & Birch‐Machin, M. A. (2018). What is the role of mitochondrial dysfunction in skin photoaging?. Experimental dermatology, 27(2), 124-128. Abstract: https://www.researchgate.net/publication/321476300_What_is_the_role_of_mitochondrial_dysfunction_in_skin_photoaging10. Koch, H., Wittern, K. P., & Bergemann, J. (2001). In human keratinocytes the Common Deletion reflects donor variabilities rather than chronologic aging and can be induced by ultraviolet A irradiation. Journal of investigative dermatology, 117(4), 892-897. Full Text: https://www.jidonline.org/article/S0022-202X(15)41393-4/fulltext11. Cioffi, F., Senese, R., Lasala, P., Ziello, A., Mazzoli, A., Crescenzo, R., … & Iossa, S. (2017). Fructose-rich diet affects mitochondrial DNA damage and repair in rats. Nutrients, 9(4), 323. Full Text: https://www.mdpi.com/2072-6643/9/4/323/htm12. Poljšak, B., & Dahmane, R. (2012). Free radicals and extrinsic skin aging. Dermatology research and practice, 2012. Full Text: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3299230/13. Rinnerthaler, M., Bischof, J., Streubel, M., Trost, A., & Richter, K. (2015). Oxidative stress in aging human skin. Biomolecules, 5(2), 545-589. Full Text: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4496685/14. Gano, L. B., Patel, M., & Rho, J. M. (2014). Ketogenic diets, mitochondria, and neurological diseases. Journal of lipid research, 55(11), 2211-2228. Abstract: https://www.ncbi.nlm.nih.gov/pubmed/2484710215. Menaa, F., Menaa, A., & Tréton, J. (2014). Polyphenols against skin aging. In Polyphenols in Human Health and Disease (pp. 819-830). Academic Press. Abstract: https://www.sciencedirect.com/science/article/pii/B978012398456200063316. Most, J., Timmers, S., Warnke, I., Jocken, J. W., van Boekschoten, M., de Groot, P., … & Blaak, E. E. (2016). Combined epigallocatechin-3-gallate and resveratrol supplementation for 12 wk increases mitochondrial capacity and fat oxidation, but not insulin sensitivity, in obese humans: a randomized controlled trial. The American journal of clinical nutrition, 104(1), 215-227. Full Text: https://academic.oup.com/ajcn/article/104/1/215/456966417. Agadjanyan, M., Vasilevko, V., Ghochikyan, A., Berns, P., Kesslak, P., Settineri, R. A., & Nicolson, G. L. (2003). Nutritional supplement (NT Factor™) restores mitochondrial function and reduces moderately severe fatigue in aged subjects. Journal of Chronic Fatigue Syndrome, 11(3), 23-36. Full Text: https://www.researchgate.net/publication/235919001_Nutritional_Supplement_NT_Factor_Restores_Mitochondrial_Function_and_Reduces_Moderately_Severe_Fatigue_in_Aged_Subjects18.Meyer, J. N., Leung, M. C., Rooney, J. P., Sendoel, A., Hengartner, M. O., Kisby, G. E., & Bess, A. S. (2013). Mitochondria as a target of environmental toxicants. Toxicological sciences, 134(1), 1-17. Full Text: https://academic.oup.com/toxsci/article/134/1/1/1666668

关注采美采购商城,
了解更多商品信息。
相关阅读